
INFORMATION
SUR L'EAU ET LA CORROSION
LA CORROSION
Définition : Norme EN ISO 8044
Interaction physico-chimique entre un métal et son environnement, entraînant des modifications dans les propriétés du métal, et souvent une dégradation fonctionnelle du métal
lui-même, de son environnement ou du système technique auquel ils appartiennent.
Ainsi, en général, la corrosion est un phénomène de nature électrochimique qui se caractérise par la mise en solution des métaux sous forme d’ions :
ANION atome possédant une charge négative par l’apport d’un ou plusieurs électrons, CATION atome possédant une charge positive par la perte d’un ou plusieurs électrons.
La plupart des métaux usuels sont chimiquement instables, et ont naturellement tendance à retourner à un état plus stable, tels qu’ils sont trouvés habituellement dans la nature,
sous forme de minerais.
La corrosion se manifeste lorsqu’il existe une différence de potentiel entre deux points, par exemple, deux métaux différents, deux zones différentes d’un même métal, deux
concentrations différentes en oxygène.
Cette différence de potentiel forme une pile dont l’anode libère les électrons cédés. Dans le cas de l’acier, le fer (anode) passe en solution. Il y a corrosion de l’acier.
DIFFÉRENTS TYPES DE CORROSION
Corrosion uniforme :
Corrosion généralisée progressant presque à la même vitesse sur l’ensemble de la surface d’un métal donné en contact avec un milieu environnant corrosif.
Corrosion localisée :
Corrosion se concentrant préférentiellement sur des sites discrets de la surface d’un métal exposé à un milieu corrosif.
FACTEURS AGGRAVANTS
• Bi ou multi-métalisme.
• État de propreté interne : calamines, graisses, corps étrangers, saletés.
• Résidus de flux de soudage et de brasage / Stagnation / Bras morts / Dépôts / Micro-
courants et courants vagabonds.
• Stress des métaux : formage, soudage, contraintes mécaniques et thermiques.
• Produits dégradés : antigels, certains inhibiteurs ou réducteurs d’O
2
, matières
organiques.
• Présence de micro-organismes : bactéries (particulièrement les sulfato-réductrices),
levures, algues.
• Éléments agressifs et corrosifs : chlorures (Cl-), sulfates (SO
4
-) et ammoniac/
ammonium (NH
3
/NH
4
+) particulièrement pour le cuivre, fluorures (F-), sodium (Na+)
ou potassium (K+) s’il y a présence d’aluminium.
• Les alcalins forts : soude, potasse, ammoniaque sont agressifs pour les plastiques et
les caoutchoucs.
• Gaz dissous : Oxygène (O
2
), Gaz Carbonique (CO
2
).
FACTEURS INFLUANT SUR LE RISQUE DE CORROSION
Matériaux métalliques :
Composition chimique, caractéristiques de la surface.
Conception et construction :
Géométrie, systèmes multi-métalliques, assemblages. Procédures avant mise en
service : essais d’étanchéité.
Nettoyage :
lessivage, rinçage.
Eau :
caractéristiques physico-chimiques, gaz dissout.
Conditions d’exploitation :
Température, conditions d’écoulement.
Autres facteurs :
Contraintes de traction, température (Dt), micro-courants.
Afin de limiter l’effet de ces facteurs, la conception, la construction, la mise en service et
l’exploitation d’une installation doivent faire l’objet de précautions particulières.
EFFETS DE LA CORROSION ET DOMMAGES
• Corrosion formation d’hydroxydes
• Boue noire magnétisable (magnétite)
• Embouage restriction du débit
• Efficacité réduite perte de rendement
• Engorgement et bouchage corrosion érosion (cuivre)
• Abrasion des joints tournants perte d’étanchéité
• Aération corrosion sous dépôts (aération différentielle, bactéries)
• Percement, perte d’eau, appoints d’eau, entartrage et corrosion.
EFFETS DE LA CORROSION DES MÉTAUX
Formations de boues oxydes
Corrosion sélective :
• Dézincification des laitons, graphitisation de la fonte
• Consommation des brasures
• Percement, fuites.
Colmatages de la pompe
• Encrassage de la roue : perte débit/pression
• Abrasion des paliers : usure, bruit
• Blocage de rotor : magnétite
Embouage entartrage de la chaudière
• Perte de rendement, gaspillage de combustible
• Bruits : de bouillage, claquements, coups sourds
• Casse chaudière par surchauffe du métal
CORROSION GALVANIQUE
CORROSION PAR PIQÛRES
CORROSION CAVERNEUSE
CORROSION SOUS DÉPÔT
CORROSION PAR AÉRATION
DIFFÉRENTIELLE
CORROSION À LA LIGNE D’EAU
CORROSION SÉLECTIVE
CORROSION
INTER GRANULAIRE
CORROSION - ÉROSION
CORROSION - CAVITATION
CORROSION SOUS CONTRAINTE
CORROSION PAR FUITE
DE COURANT ET PAR COURANTS
VAGABONDS
CORROSION MICRO-BIOLOGIQUE
ET BACTÉRIENNE
La vitesse de corrosion est toujours
fonction du rapport :
SURFACE CATHODIQUE
SURFACE ANODIQUE
Accroissant
la température
du métal côté fumée
amenant un grillage
ou la fêlure du métal.
700
600
500
400
300
200
100
0
1
2 3
4 5 6 7
8 9 10
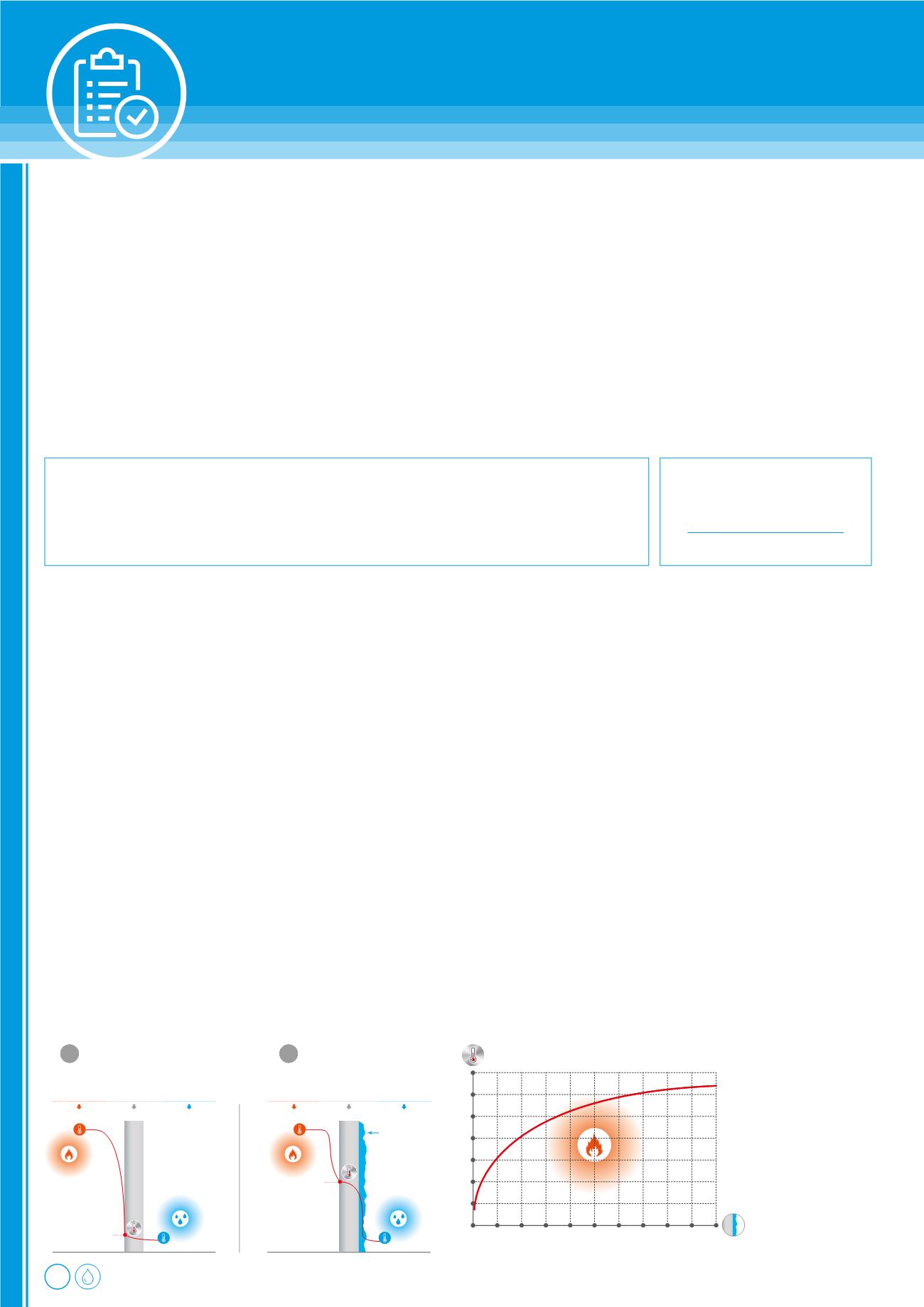
Épaisseur de tartre (mm)
Température du métal côté fumée (°C)
EFFET ISOLANT DES DÉPÔTS
CHAMBREACIER
Tôlede6mm
CÔTÉFUMÉE
110°C
800°C
80°C
CÔTÉEAU
TÔLE DE 6mm SANS TARTRE
1
456°C
3mmde tartre
800°C
80°C
CHAMBREACIER
Tôlede6mm
CÔTÉFUMÉE
CÔTÉEAU
TÔLE DE 6mm AVEC TARTRE
2
156
















